Украинский гомеопатический ежегодник: Оценка антиоксидантной активности препарата "Меркурид" на начальных этапах свободнорадикального окисления.

|
Поиск:
Гомеопатия - это...
Карта сайта
Написать письмо врачам
Написать письмо в аптеку
Правила записи на консультации врачей
Публикации по гомеопатии
Materia Medica динамизированных лекарственных препаратов...
История и практика использования биотерапевтических средств...
Гомеопатические средства в неврологии и медицинской реабилитации...
Препараты из насекомых...
Периодические профессиональные издания
Международные новости
Семинары, конференции, форумы
Одесские Гомеопатические Конгрессы
И снова о фаршированной рыбе
Объявления для гомеопатов
События, даты, поздравления и комментарии
Книги и журналы для гомеопатов
Новые издания по гомеопатии
Одесское гомеопатическое общество
Анкеты консультантов и лекторов Общества
Одесская гомеопатическая аптека
История аптеки
Номенклатура динамизированных средств
Монокомпонентные средства
Сверхвысокие разведения ГЛС
Многокомпонентные динамизированные средства
Изготовление гомеопатических лекарств
История гомеопатии в регионе
Materia medica
Гомеопатия для чайников
Вопрос - ответ
Дружественные сайты
|
ОЦЕНКА АНТИОКСИДАНТНОЙ АКТИВНОСТИ ПРЕПАРАТА «МЕРКУРИД»
НА НАЧАЛЬНЫХ ЭТАПАХ СВОБОДНОРАДИКАЛЬНОГО ОКИСЛЕНИЯ
С.Н. Гусев, А.В. Артёмов, В.П. Страшинская, С.Г. Парфентиева
Украина, г. Одесса Отдел патоморфологии и
иммунологии Украинского НИИ глазных болезней и тканевой
терапии им. В.П. Филатова The estimation of antioxidant
activity of the preparation «Mercurid» at the initial stages of free radical
oxidation. S.N. Gusev, A.V. Artemov, V.P. Strashinskaja, S.G. Parfentieva ( The article presents general notions
about processes of free radical oxidation, systematizes the application of
metal compounds in medicine, and stated scientific-experimental researches of
antioxidant activity of the preparation «Mercurid». On the basis of their own experience,
the authors concluded that allopathic and homeopathic forms of «Mercurid» are
perspective in treatment of inflammatory diseases, in preventive maintenance of
complications after chemotherapeutic treatment, in detoxication, in decrease of
damages of DNA caused by oxidizing stress, in atherosclerosis and ischemic
diseases of various localization. Ключевые
слова: «Меркурид»,
антиоксидантная активность, эксперимент, соединения ртути, свободнорадикальное
окисление, гомеопатические лекарственные формы Общие
представления о процессах свободнорадикального окисления Избыточная активация реакций
свободнорадикального окисления представляет типичный патологический процесс,
присущий самым различным заболеваниям и повреждающим воздействиям на организм.
Свободные радикалы – молекулы с неспаренными электронами, находящимися на
внешней оболочке атома или молекулы, обладающие очень высокой реакционной
способностью и, как следствие, выраженным повреждающим действием на клеточные
макромолекулы. Доказано участие свободных радикалов в патогенезе очень многих
заболеваний (шок различного генеза; атеросклероз; нарушения мозгового,
коронарного и периферического кровообращения; сахарный диабет и диабетическая
ангиопатия; ревматоидные, воспалительные и дегенеративные заболевания
опорно-двигательной системы; поражения глаз; заболевания лёгких; онкологическая
патология; термические поражения; различные интоксикации; реперфузионные
поражения) и преждевременного старения. Кроме того, к повышенному образованию
свободных радикалов в организме ведут: приём препаратов с прооксидантными
свойствами, проведение ряда лечебных процедур (кислородотерапия,
гипербарическая оксигенация, ультрафиолетовое облучение, лазерная коррекция
зрения, лучевая терапия), а также различные экологически неблагоприятные факторы
окружающей среды. Механизм свободнорадикального окисления и
связанную с ним антиоксидантную систему рассматривают как важнейшее
патогенетические звено многих патологических процессов. От этого механизма в
значительной степени зависит структурно-функциональная целостность клеток и
тканей организма, что напрямую сопряжено с воспалительными процессами, а также
старением и опухолевой трансформацией. Свободнорадикальное окисление обусловлено
активными формами кислорода, образующимися в результате ферментативной
деятельности оксиредуктазы. При этом образуются ионы кислорода и перекись
водорода. Определённую роль в этом процессе играет
аутоокисление катехоламинов. Механизм повреждающего действия реализуется через
взаимодействие ионов кислорода и перекиси водорода с образованием гидроксильных
радикалов и свободного кислорода. Это приводит в инактивации различных белков,
деструктивным изменениям полисахаридов и стимуляции мутагенеза за счёт
повреждения ДНК. Активные формы кислорода инициируют
перекисное окисление жирных кислот и их дериватов, что приводит к образованию
карбонильных соединений, связывающихся с нуклеиновыми кислотами и белками. Как видно, антиоксидантная защита может
стать важным фактором на пути мутагенных изменений, ведущих к образованию
неопластических клеток и опухолевой прогрессии. С целью воздействия на свободнорадикальное
окисление в последнее время стали применять антиоксиданты в лечении ишемических
заболеваний различной локализации. Широкое применение нашли такие вещества с
антиоксидантной активностью, как α-токоферол, дибутинол, оксипиридины. Однако многие известные антиоксиданты
имеют серьёзные недостатки: они действуют лишь на конечном этапе
свободнорадикального окисления, а при разложении свободных радикалов
полиненасыщенных жирных кислот образуют токсичные продукты (см. табл.1). В связи со сказанным, поиск более
эффективных антиоксидантов является актуальной проблемой. Применение
соединений металлов в медицине Применение соединений металлов в медицине имеет длительный опыт.
Металлы считают главными факторами металлообразования и функционирования
активных центров большинства ферментов [8,9]. Для каждого биометалла по
диаграмме Бертрана [6] (зависимость «доза элемента – физиологическое действие»)
существует диапазон оптимальных концентраций in vivo, выход за пределы которых
обусловливает нарушение ферментного статуса организма (дефицит элемента) или
токсическое влияние (превышение депообразующей потребности в элементе). Поэтому
путём к повышению биодоступности и безопасности металлосодержащих препаратов
может быть замена ионных соединений микроэлементов их комплексами с
органическими лигандами [4,7]. Подтверждение этого нашло свое отображение в
работе Института фармакологии и токсикологии АМН Украины «Комплексообразование
как способ повышения безопасности соединений микроэлементов» (Григорьева Г.С.,
Киричок Л.М., Конахович Н.Ф., Мисливець С.О., Мохорт Н.А.). Рациональность
такого подхода была реализована и при создании препарата «Меркурид». Общеизвестно, что максимальную токсичность проявляют наиболее химически
активные частицы, координационноненасыщенные ионы, к числу которых следует отнести
ионы свободных металлов. Снижение электрофильных свойств иона соответственно
приводит к снижению его токсического действия на организм. Хелатирование
свободных ионов металла полидентатными лигандами превращает их в устойчивые,
координационно насыщенные частицы, не способные разрушить биокомплексы, а,
следовательно, малотоксичные. Они мембранопроницаемы, способны к
транспортировке и выведению из организма. Научно-экспериментальные исследования
антиоксидантной активности препарата «Меркурид» Объектом исследования стал
препарат «Меркурид» – хелатный комплекс ртути с α-аминокислотами – цистеином
или метионином. При приёме «Меркурида» микродозы ртути находятся в связанном
состоянии с аминокислотами (хелатный комплекс), и в концентрации, безвредной
для организма, оказывают биотическое воздействие на ряд жизненно важных процессов.
Для подтверждения этого тезиса были проведены исследования острой и хронической
токсичности «Меркурида». Острую токсичность изучали на базе
Национального фармацевтического университета (Харьков). Базовый препарат
«Меркурид» (сток), в соответствии с классификацией веществ по токсичности,
отнесен к 4 классу токсичности (малотоксические вещества, 501<LD50<5000
мг/кг). Изучение хронической токсичности было
проведено отделом патоморфологии и иммунологии Украинского НИИ глазных болезней
и тканевой терапии им. В.П. Филатова. Отчёт об изучении хронической токсичности
позволяет сделать следующие обобщения. Сток «Меркурида», при применении в
10-кратной терапевтической дозе на протяжении 2 месяцев, не вызывает
токсических изменений в организме крыс. При гистоморфологическом исследовании
патологии не выявлено. Одним из механизмов такого действия, как
показали наши предыдущие исследования, является влияние на тиолдисульфидные
связи протеинов. Происходящее при этом изменение белкового редокс-потенциала
сопровождаеют конформационные изменения белков и, в частности, связанных с
процессами иммуногенеза и онкогенеза. Итогом этих изменений, как показали
наблюдения, является повышение цитостатической активности клеток иммунной
системы и активация апоптоза опухолевых клеток. Отмеченные свойства «Меркурида», как мы
полагаем, в значительной степени связаны с имеющейся в комплексном соединении
ртутью. Участие лишь аминокислотных компонентов «Меркурида» в конформационном
воздействии на белки маловероятно. В то же время, как самостоятельно, так и в
хелатном комплексе, цистеин и метионин могут выступать компонентами антиоксидантной
системы. Ранее проведенные исследования «Меркурида» показали наличие у него
противовоспалительных, противоопухолевых, противовирусных и иммуномодулирующих
свойств (патент Украины №55308А). Представляет интерес оценка
антиоксидантной активности «Меркурида», учитывая, что свободнорадикальное
окисление играет важную роль в онкогенезе. Следует также отметить, что изучение
свободнорадикальных повреждений и разработка антиоксидантной защиты в процессе
химиотерапевтического лечения онкологических больных, уже привлекли внимание
онкологов. Мы полагаем, что роль антиоксидантов не менее важна также для
профилактики ранних и поздних рецидивов (как лекарственных средств
сопровождения адъювантной и неадъювантной терапии). В данной работе нами использован
усовершенствованный метод оценки антиокислительной активности антиоксидантов на
начальных этапах свободнорадикального окисления по ингибированию
супероксидрадикала в реакции аутоокисления адреналина в адренохром в щелочной
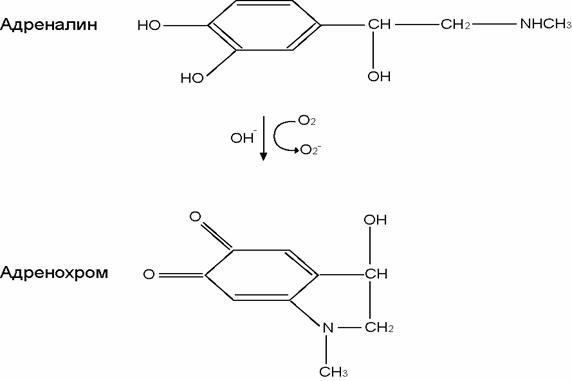
среде (рис.1). [if gte vml 1]> Рис.1. Схема аутоокисления адреналина в адренохром Материалы и
методы
В кювету (объёмом 10 мл) спектрофотометра
СФ-26 вносили 2,0 мл 0,15 М натрий-карбонатного буфера, с добавлением 3·10-4
мл ЭДТА (рН=10,2), затем прибавляли растворы исследуемых препаратов. Реакцию
начинали прибавлением 0,4 мл 2,25·10-3 М водного раствора адреналина.
Исходный кристаллический адреналин растворяли в дистиллированной воде и доводили
разбавленной хлороводородной кислотой до рН=2,25. Сначала определяли показатель
экстинкции (Е1), отражающий скорость ингибирования аутоокисления
адреналина, а затем показатель экстинкции (Е2), отражающий скорость
аутоокисления адреналина в присутствии исследуемых препаратов. Реакцию проводили
при Т=35-36°С в спектрофотометре СФ-26, при длине волны λ-480 нм; время
экстинкции – 3 мин. Антиокислительную активность исследуемых препаратов выражали
в процентах (%) ингибирования аутоокисления адреналина, и вычисляли по формуле: Е1 – Е2 х 100 Е1 Статистическую обработку проводили с
использованием t-критерия Стьюдента. Различие достоверно по сравнению с
контролем Р≤0,001. Результаты и обсуждение В данной работе, для оценки антиоксидантной активности
по ингибированию супероксидрадикала в реакции аутоокисления адреналина в аденохром,
нами использованы базовые хелатные соединения ртути с аминокислотами (стоки),
которые служат в дальнейшем для приготовления гомеопатических препаратов (по
Фармакопее Швабе): 1. Комплекс ртути с цистеином, обозначенный
Меркурид Ц (сток); 2. Комплекс ртути с метионином, обозначенный
Меркурид М (сток); 3. Этилендиаспарагинат Hg(II), (хим.
формула C10H10O8N2Hg), обозначенный
Меркурид Ас – новое соединение, полученное авторами, находящееся в стадии
исследования и патентования; 4. Гомеопатический препарат, полученный от стока
Меркурид Ц в разведении С6, и обозначенный Меркурид Ц, С6 (гомеопатический); 5. Гомеопатический препарат, полученный от
стока Меркурид М в разведении С6, и обозначенный Меркурид М, С6
(гомеопатический); В качестве препаратов сравнения
использованы широко известные препараты антиоксидантного действия - α-токоферол
и диметилсульфоксид, являющиеся одними из наиболее сильных реактиваторов
супероксиддисмутазы. Хотя указанные препараты получили достаточно широкое
распространение в медицинской практике, они обладают побочными эффектами. Поэтому
поиск новых лекарств, лишённых таких свойств, остаётся актуальной задачей. Статистическую обработку проводили с
использованием t-критерия Стьюдента. Различие достоверно по сравнению с
контролем Р≤0,001. Анализ представленных данных позволяет
говорить о наличии антиоксидантной активности у всех исследовавшихся препаратов
группы Меркурид. Причём, эта активность выше, чем у известного антиоксиданта
α-токоферола (гомеопатический препарат Меркурид в разведении С6 более чем
в три раза превышает антиоксидантную активность α-токоферола). Таблица 1
Таблица 2 Сравнительная
характеристика антиокислительной активности стоков Меркурида и гомеопатических
лекарств на его основе Меркурида Ц и М в разведении С6
Важно отметить, что гомеопатические разведения (Меркурид С6) показали
более высокую антиоксидантную активность в сравнении с аллопатическими
аналогами (стоками). Возможно, это обусловлено тем, что при высоких степенях
динамизации происходит запоминание химических связей, аминокислоты
освобождаются от координационного влияния атома ртути и проявляют действие,
связанное с наличием атома серы в своём составе. Таким образом, результаты исследования
препаратов группы Меркурид показали, что их можно рассматривать как лекарственные
вещества с очевидной антиоксидантной активностью неферментного характера. Учитывая различия в уровнях
антиоксидантной активности и влияниях на тиолдисульфидные белковые связи,
«Меркурид», рационально назначать при воспалительных заболеваниях или в
комплексном лечении онкологического процесса (профилактика рецидивов и последствий лучевой терапии,
химиотерапии). Учитывая
антиоксидантную активность и физиологическое влияние на тиолдисульфидные
белковые связи, аллопатические и гомеопатические формы Меркурида следует рассматривать
перспективными для лечения воспалительных заболеваний, профилактики осложнений
после химиотерапевтического лечения, дезинтоксикации, уменьшения повреждений ДНК
(вызванных окислительным стрессом), атеросклероза, ишемических заболеваний
различной локализации. БИБЛИОГРАФИЯ: 1. Бойцова Л.В. Изменение антиоксидатной системы
глутатиона как показатель цитотоксического действия платидиама // Інститут фармакології та
токсикології АМНУ (Київ). 2. Дунаев В.В., Беленичев И.Ф., Ковеленко С.И. и др.
Антиорадикальная и антиокислительная активность производных 1,2,4-триазола и
хиназола при ишемии головного мозга // Украинский биохимический журнал. – 1996.
– Т.68 (№1). – С.100-103. 3. Зайцев В.Г., Закревский В.И. Защита клеток от
экзогенных и эндогенных активных форм кислорода: Методические подходы к
изучению // Фундаментальные и прикладные аспекты современной биохимии: Тр.
научной конференции, посвященной 100-летию кафедры биохимии Санкт-Петербургского
медицинского университета им. акад. И.П. Павлова. – СПб., 15-17.10.1998 года,
СПб., 1998. – Т.2. – С.401-405. 4. Координационные соединения металлов в медицине / Е.Е.
Крисс, И.И. Волченскова, А.С. Григорьева, К.Б. Яцимирский, Л.И. Бударин. –
Киев: Наукова думка, 1986. 5. Коровина Н.А., Захарова И.Н., Обыночная Е.Г. Применение
антиоксидантов в педиатрической практике // Consilium medicum. – 2003. – Т.5
(№9). 6. Попова И.Ю., Лазарева Д.Н., Зарудный Ф.С. //
Экспериментальная клиническая фармакология. – 1996. – Т.59 (№3). – С.72-77. 7. Kemp J.D. // Journal Clinical Immune. – 1999. – V.13
(№2). – P.81-89. 8. Metal ions in biological systems: In 23 vols / Ed.
H.Sigel. – N.-Y.; Basel: Dekker, 1975-1994. 9. Trace elements in human and animal nutrition. – 5th
ed. / Ed. W.Mertz. – San Diego, California: Academic Press, 1987. Оценка антиоксидантной активности препарата «Меркурид» на начальных этапах
свободнорадикального окисления. С.Н. Гусев, А.В. Артёмов, В.П. Страшинская,
С.Г. Парфентиева (Одесса, Украина) В статье даны общие
представления о процессах свободнорадикального окисления, систематизировано
применение соединений металлов в медицине, изложены научно-экспериментальные
исследования антиоксидантной активности препарата «Меркурид». На основе
собственного опыта, авторы делают вывод, что аллопатические и гомеопатические
формы «Меркурида» следует рассматривать перспективными для лечения
воспалительных заболеваний, профилактики осложнений после химиотерапевтического
лечения, дезинтоксикации, уменьшения повреждений ДНК (вызванных окислительным
стрессом), атеросклероза, ишемических заболеваний различной локализации. Оцінка
антиоксидатної активності препарату «Меркурід» на початкових етапах
вільнорадикального окислення. С.М. Гусєв, О.В. Артьомов, В.П. Страшинська, С.Г.
Парфентієва (Одеса, Україна) У статті надані загальні уявлення про процеси вільнорадикального окислення,
систематизовано застосування сполук металів в медицині, викладені науково - екпериментальні
дослідження антиоксидантної активності препарату «Меркурід». На підставі
власного досвіду, автори роблять висновок, що алопатичні та гомеопатичні форми
Меркуріду слід розглядати перспективними для лікування запальних захворювань,
профілактики ускладнень після хіміотерапевтичного лікування, дезінтоксикації,
зменшення ушкоджень ДНК (що спричинені окислювальним стрессом), атеросклерозу,
ішемічних захворювань різної локалізації. Информация об авторах: участник и дипломант международных профессиональных
форумов, автор более 20 публикаций Сергей Николаевич Гусев – автор лекарства
«Меркурид», кандидат медицинских наук Александр Валентинович Артёмов, и их
коллеги. Украина, г. Одесса, ул. Старопортофранковская 101, тел.(0482)320-210,
e-mail: mercurid@te.net.ua,
www.mercurid.com | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||